- 010-68321050
- 搜索
- 企業(yè)郵箱
- 產(chǎn)品定制

專(zhuān)屬客服號(hào)

微信訂閱號(hào)
全面提升數(shù)據(jù)價(jià)值
賦能業(yè)務(wù)提質(zhì)增效
摘要:近年來(lái),醫(yī)改逐漸向縱深推進(jìn),“仿制藥一致性評(píng)價(jià)”、“限制輔助性用藥”、“醫(yī)保控費(fèi)”、“兩票制”等對(duì)醫(yī)藥行業(yè)影響重磅政策相繼出臺(tái)。特別是最近的“4+7帶量采購(gòu)”政策的推出,使傳統(tǒng)營(yíng)銷(xiāo)驅(qū)動(dòng)下的仿制藥企業(yè)面臨巨大的生存壓力,之前粗狂式發(fā)展的紅利期基本結(jié)束,創(chuàng)新驅(qū)動(dòng)的產(chǎn)品為王時(shí)代即將到來(lái),醫(yī)藥產(chǎn)業(yè)的轉(zhuǎn)型升級(jí)成為發(fā)展的必然趨勢(shì)。
創(chuàng)新藥已成為醫(yī)療健康產(chǎn)業(yè)當(dāng)前的熱門(mén)話題,從國(guó)家政策的改革和鼓勵(lì),企業(yè)意識(shí)的覺(jué)醒和投入,資本的關(guān)注和追捧,海外人才的大量回流,生物技術(shù)的日新月異,整個(gè)行業(yè)的氛圍都在為創(chuàng)新鋪路,我國(guó)創(chuàng)新藥研發(fā)的戰(zhàn)略短期不會(huì)改變,國(guó)內(nèi)藥企對(duì)新藥的研發(fā)投入將持續(xù)增加。
新藥研發(fā)流程及產(chǎn)業(yè)鏈概況
醫(yī)藥行業(yè)流傳著一句話,新藥的上市有兩個(gè)十,十年的時(shí)間和十億資金的投入,一般是“萬(wàn)里成一”,是一個(gè)集資金、技術(shù)和“運(yùn)氣”密集較高的行業(yè)。新藥研發(fā)的過(guò)程要面對(duì)大量錯(cuò)綜復(fù)雜和互相矛盾的數(shù)據(jù),每個(gè)細(xì)微的決定都可能使多年的努力付之東流,使公司長(zhǎng)時(shí)間陷入進(jìn)退兩難的困境。
新藥研發(fā)的首要工作是要確定藥物的生物標(biāo)記及作用靶點(diǎn),篩選化合物并將其優(yōu)化作為候選藥物,進(jìn)入開(kāi)發(fā)階段;開(kāi)發(fā)階段的首要任務(wù)是要對(duì)候選藥物進(jìn)行毒理學(xué)研究,并向國(guó)家藥監(jiān)局提交試驗(yàn)用新藥(IND)申請(qǐng),這個(gè)階段需要各個(gè)學(xué)科的協(xié)作,比如合成工藝、藥代動(dòng)力學(xué)、藥理學(xué)、制劑等各學(xué)科的協(xié)作;然后進(jìn)入臨床試驗(yàn)階段,這個(gè)階段要向藥監(jiān)局提交新藥IND,臨床I期需要在健康人身上進(jìn)行試驗(yàn),臨床II期需要在相關(guān)病人身上進(jìn)行試驗(yàn),臨床III期是II期的大范圍驗(yàn)證階段也是為藥品注冊(cè)申請(qǐng)獲得批準(zhǔn)提供依據(jù)的關(guān)鍵階段,光是臨床試驗(yàn)要花費(fèi)新藥開(kāi)發(fā)70%以上的費(fèi)用。
完成以上階段的試驗(yàn)并分析所有的數(shù)據(jù)和資料,藥物的有效和安全性得到證明后,新藥持有人則可以向藥監(jiān)局提交新藥上市的申請(qǐng)。詳情請(qǐng)見(jiàn)圖1。
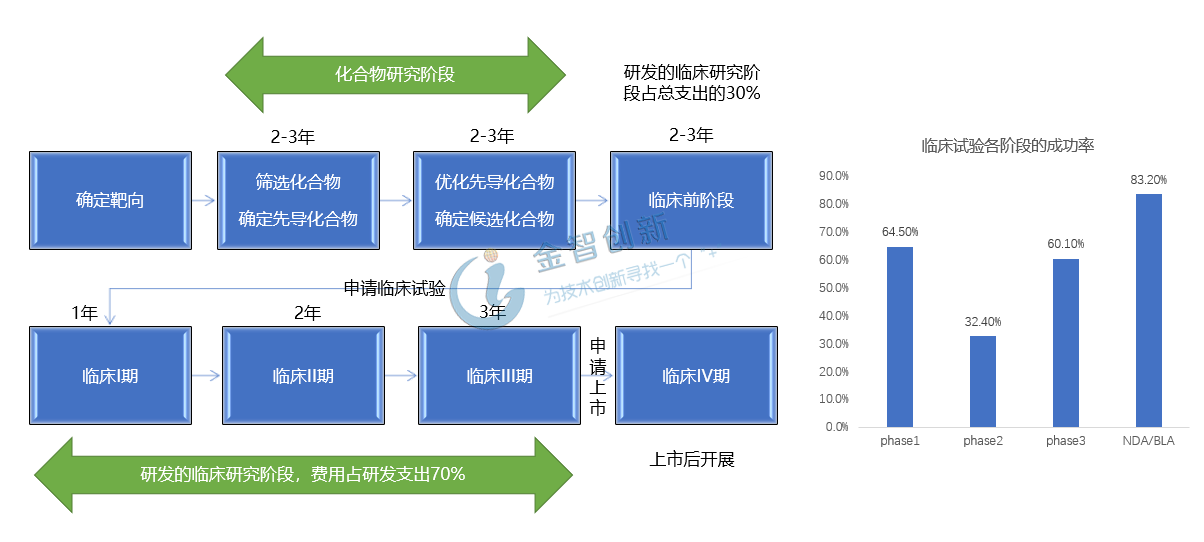
圖1 新藥研發(fā)流程及各階段的成功率
(資料來(lái)源:五度易鏈行業(yè)研究中心,Nature Biotechnology)
新藥的研發(fā)興起促進(jìn)了產(chǎn)業(yè)鏈的發(fā)展,出現(xiàn)研發(fā)外包服務(wù)的細(xì)化分工,根據(jù)研發(fā)階段的不同,外包服務(wù)一般分為合同研發(fā)服務(wù)(CRO)、合同生產(chǎn)業(yè)務(wù)(CMO)和合同銷(xiāo)售組織(CSO),分別對(duì)應(yīng)新藥研發(fā)領(lǐng)域中的臨床前研究及臨床研究、定制化生產(chǎn)及研發(fā)服務(wù)、醫(yī)藥流通等產(chǎn)業(yè)鏈中的不同環(huán)節(jié)。詳情見(jiàn)圖2。
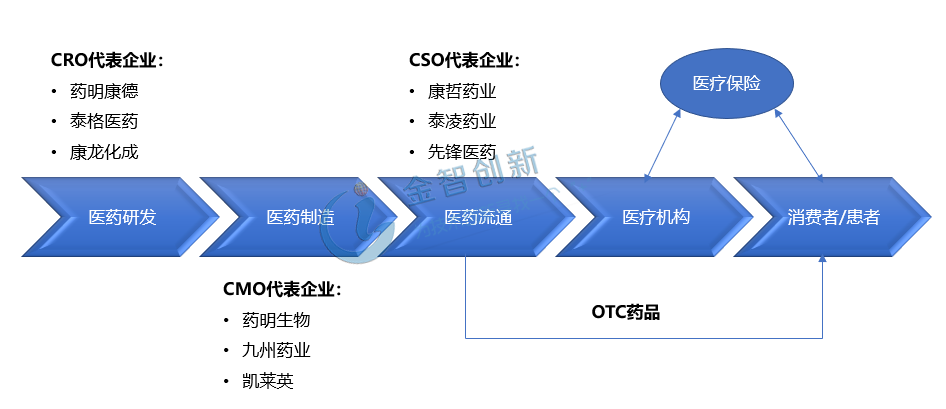
圖2 新藥研發(fā)產(chǎn)業(yè)鏈
(資料來(lái)源:公開(kāi)資料整理,五度易鏈行研)
我國(guó)藥物研發(fā)升級(jí)的路線
我國(guó)藥物的研發(fā)歷程主要分為四個(gè)階段,第一階段是1950至1985年的跟蹤仿制階段,以滿足生命衛(wèi)生安全為最基本的要求;第二階段為1985-2000年的新藥研發(fā)初期階段,該階段的產(chǎn)品仍以仿制藥為主,初有新藥研發(fā)的技術(shù)和意識(shí);第三階段為2000-2015年的新藥研發(fā)崛起階段,新藥研究開(kāi)始轉(zhuǎn)入以新化學(xué)結(jié)構(gòu)為主要目標(biāo)的階段;第四階段為2015年以后,國(guó)家地區(qū)政策多方面支持,開(kāi)創(chuàng)我國(guó)新藥研究的第三個(gè)階段—First in class階段。詳情如圖3所示。
 圖3 我國(guó)創(chuàng)新藥研發(fā)升級(jí)路線
圖3 我國(guó)創(chuàng)新藥研發(fā)升級(jí)路線
(資料來(lái)源:公開(kāi)整理,五度易鏈行研)
現(xiàn)階段,我國(guó)新藥研發(fā)已經(jīng)啟動(dòng)由單純仿制(1.0版)向?qū)@?2.0版)以及自主創(chuàng)新海外協(xié)同發(fā)展的(3.0版)升級(jí)通道。仿藥的市場(chǎng)機(jī)會(huì)相對(duì)較少,首創(chuàng)藥(FIC)一般占據(jù)市場(chǎng)份額的80%左右。而且隨著進(jìn)口藥在我國(guó)上市的時(shí)間縮短,國(guó)內(nèi)Me too類(lèi)創(chuàng)新藥的風(fēng)險(xiǎn)將大大提高,這類(lèi)新藥需要有不同于原研藥的亮點(diǎn),才可能提高自身的價(jià)值。
國(guó)內(nèi)創(chuàng)新藥研發(fā)集群及2019年藥品研發(fā)公司排行榜
研發(fā)是生物醫(yī)藥產(chǎn)業(yè)的創(chuàng)新源頭和立身之本,厚植研發(fā)優(yōu)勢(shì),形成創(chuàng)新集群。我國(guó)創(chuàng)新藥研發(fā)按照大方向來(lái)分包括四大產(chǎn)業(yè)集群,包括大企業(yè)集群、創(chuàng)新型小公司集群、專(zhuān)業(yè)研發(fā)公司集群、科研院所集群。大企業(yè)集群是以恒瑞醫(yī)藥、石藥集團(tuán)等實(shí)力龐大的集團(tuán)性公司群體,創(chuàng)新型小公司集群是科創(chuàng)板上市的微芯生物為代表的小公司,專(zhuān)業(yè)研發(fā)公司集群的代表公司為華領(lǐng)醫(yī)藥和歌禮生物,科研院所集群是中科院上海藥物研究所、中國(guó)醫(yī)科大學(xué)、沈陽(yáng)醫(yī)藥大學(xué)等。
2019中國(guó)醫(yī)藥健康產(chǎn)業(yè)發(fā)展大會(huì)發(fā)布《2019中國(guó)藥品研發(fā)實(shí)力排行榜》,百?gòu)?qiáng)企業(yè)領(lǐng)銜控半壁江山,而2019年總榜十強(qiáng)企業(yè),是行業(yè)發(fā)展前沿的縮影,憑借企業(yè)獨(dú)家品種、研發(fā)資源、規(guī)模效應(yīng)等方面的優(yōu)勢(shì)在發(fā)展中搶跑。其中恒瑞醫(yī)藥、正大天晴、齊魯制藥、復(fù)星醫(yī)藥、科倫藥業(yè)5企業(yè)4年均位列前10。如表1所示。
表1 2019中國(guó)藥品研發(fā)實(shí)力前十強(qiáng)
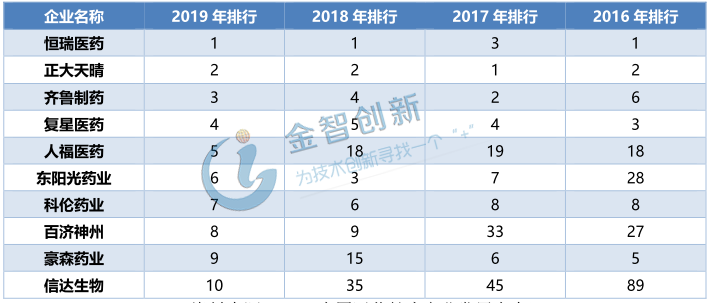
(資料來(lái)源:2019中國(guó)醫(yī)藥健康產(chǎn)業(yè)發(fā)展大會(huì))
總結(jié)
綜上所述,新藥的上市歷程異常艱難,需要十年的時(shí)間和十億的資金來(lái)支撐,研發(fā)階段的每個(gè)決策都影響著研發(fā)的停止,很容易讓公司陷入進(jìn)退兩難的地步,即便如此,各個(gè)醫(yī)療公司每年還不停的加大研發(fā)投入,可見(jiàn)市場(chǎng)的熱度。隨著我國(guó)新藥研發(fā)的不斷升級(jí),留給仿藥市場(chǎng)的份額越來(lái)越少,未來(lái)創(chuàng)新驅(qū)動(dòng)的產(chǎn)品為王時(shí)代即將到來(lái)。
本文為我公司原創(chuàng),歡迎轉(zhuǎn)載,轉(zhuǎn)載請(qǐng)標(biāo)明出處,違者必究!


請(qǐng)完善以下信息,我們的顧問(wèn)會(huì)在1個(gè)工作日內(nèi)與您聯(lián)系,為您安排產(chǎn)品定制服務(wù)
評(píng)論