
專屬客服號

微信訂閱號
全面提升數據價值
賦能業務提質增效
摘要:雖然近些年全球醫藥企業相關研發投入增加,但研發成功率降低、研發周期變長,而作為醫藥行業研發專業化分工的產物,CRO企業憑借其高效率、低成本、服務廣等特點,迅速發展,目前已經成為醫藥研發產業鏈中不可或缺的重要環節,覆蓋了藥物研發的全過程。
CRO(合同研究組織)是藥物研發風險平均化和研發分工專業化的產物,目前已逐步發展為國際醫藥研發外包的常用模式。CRO涵蓋了新藥研發的全過程,根據服務階段不同,可以分為臨床前及臨床試驗CRO和化合物研究CRO兩大類,CRO的出現極大的促進了全球新藥研發。
新藥研發難度加大,醫藥外包大行其道
近十幾年內,隨著政府監管要求日益嚴格,基礎試驗費用日漸增加、臨床試驗規模逐步擴大、臨床試驗失敗率相應提高,多項因素導致新藥研發成本迅速增長,給醫藥企業的經營帶來巨大壓力。面對這種困境,制藥企業開始重新規劃戰略,由過去的“研、產、銷”的全產業鏈模式,轉變為現在的“銷”,將工作的重點轉移到資源運作和整合上,藥物的研發和生產環節對企業的生存發展也有著重要的作用,而CRO模式的出現使醫藥企業能夠在藥物研發和生產的環節上繼續保持控制力,無需投入太多精力。CRO企業由于擁有藥企相對薄弱的優勢,如人才、設備、換證招募等方面的優勢,研發外包逐漸成為一種重要的研發模式,并且被越來越多制藥企業所接受。
醫藥CRO外包平均可以將臨床試驗的時間縮短20%-30%,同時可以將風險分散在研發產業鏈的各個環節,研發投入相對降低,制藥企業的風險得到部分轉移。尤其是近年來國外興起的CRO企業與藥企之間“風險共擔、收益共享”的新藥研發模式,則進一步降低了藥企的研發風險。
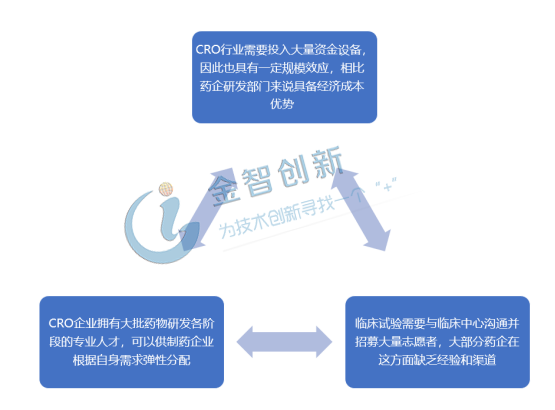
圖1 CRO企業在醫藥研發產業中的優勢
(資料來源:五度易鏈行業研究中心)
新藥審批量的增加和研發支出的增長為CRO 行業的持續增長奠定基礎
從全球范圍的醫藥CRO發展來看,受全球尤其是美國對藥物研發的重視及藥品專利到期的影響,新藥審批量逐漸從低谷走出,新藥審批量的增加為CRO 行業的持續增長奠定基礎。以美國為例,據Frost & Sullivan數據顯示,2018年美國FDA共批準61種藥物,其中兩種是由CBER批準,其余的59種由CDER批準,比2017年新藥審批數量增加14種,是近十年內新藥批準的高峰。除了獲批新藥數量龐大外,新藥的質量也讓2018年成為制藥行業的分水嶺。詳情請見圖2。
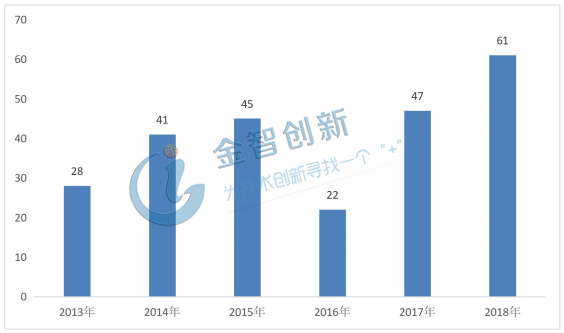
圖2 美國歷年新藥審批量
(資料來源:Frost & Sullivan,五度易鏈行研整理)
Frost & Sullivan數據顯示,2018年全球醫藥研發支出高達1510美元,與2017年研發支出增長3.4%,保守估計未來以2%的增長率增長,預計2021年的全球醫藥研發支出將達到1600億美元,詳情請見圖3。新藥研發支出的增長也為CRO行業的增長帶來新的機遇。
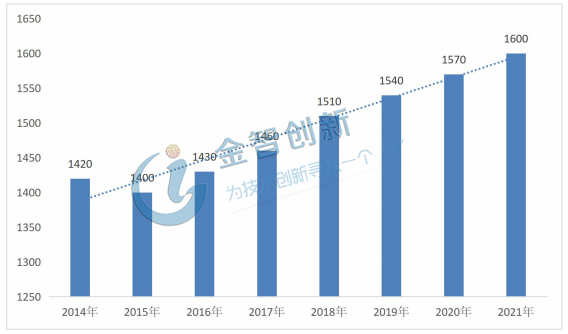
圖3 全球新藥研發支出詳情(單位:億美元)
(資料來源:Frost & Sullivan,五度易鏈行研整理)
醫藥研發外包服務大幅拓寬,2021年全球CRO市場規模將達479億美元
目前醫藥研發外包服務業務已由最初的藥物發現、臨床前研究、藥物基因組學、藥物安全性評價等有限服務發展到幾十項內容,甚至包括數據管理與分析、信息學、政策法規咨詢、產品注冊、生產和包裝、推廣、市場、產品發布和銷售支持以及各類相關的商業咨詢等諸多領域,而且每年都有新的服務內容增加,醫藥研發領域外包服務的范圍已大幅拓寬。
隨著新藥研發難度的加大,以及不斷增長的全球制藥行業(已批準了越來越多的新藥)和近年來藥物研究與開發的高額支出,為全球合同研究組織(CRO)市場帶來了福音。據美通社報道顯示全球醫藥CRO行業規模持續增長約8%,2018年全球市場規模高達371億美元,與去年相比增長約6%,未來三年將持續增長,預計2021年全球CRO市場規模將達479億美元。詳情請見圖4。
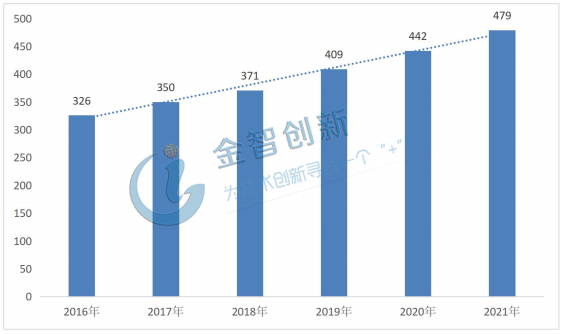
圖4 全球CRO行業市場規模情況(單位:億美元)
(資料來源:美通社)
結語
綜上所述,由于近十幾年政府對藥物監管要求日益嚴格,以及不斷增長的全球制藥行業(已批準了越來越多的新藥)和近年來藥物研究與開發的高額支出等多因素導致新藥的開發成本迅速增長,給醫藥企業的研發帶來壓力,同時為全球合同研究組織(CRO)市場帶來了福音,被越來越多制藥企業所接受,預計2021年全球CRO市場規模將達479億美元。如此的市場規模與藥物研發投入相比,還有很大增長空間,所以CRO行業未來的崛起只是時間問題。
本文為我公司原創,歡迎轉載,轉載請標明出處,違者必究!


請完善以下信息,我們的顧問會在1個工作日內與您聯系,為您安排產品定制服務
評論