
專屬客服號

微信訂閱號
全面提升數據價值
賦能業務提質增效
近年來,在特別審批、突破性治療藥物、附條件批準、優先審評審批等藥品加快上市注冊程序下,國內外新藥快速進入中國市場。
據統計,僅2022年上半年,國內就有13款原創新藥獲批上市并有望進入今年的醫保目錄,包括國產1類新藥8款,進口1類新藥3款,以及2款按特別審批程序附條件批準的新冠藥物,詳情見下表。
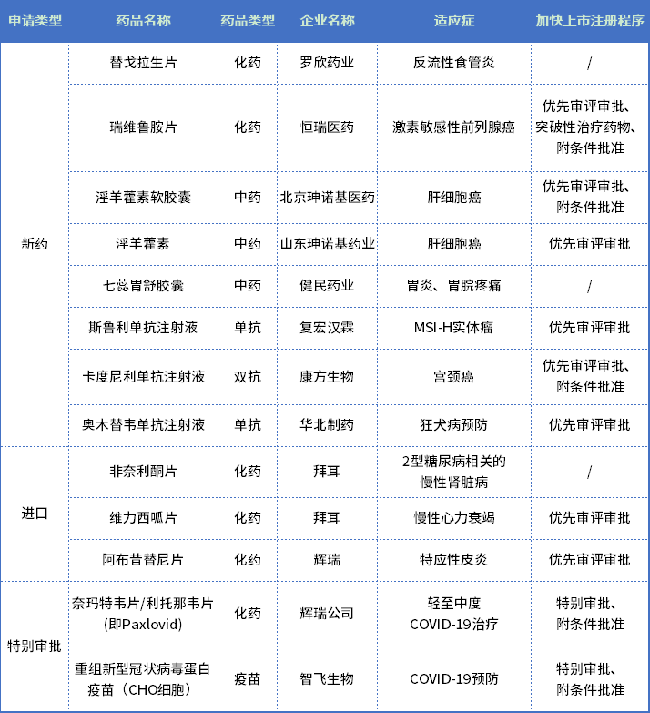
表1 2022上半年獲批上市的新藥
從適應癥來看,抗腫瘤藥備受青睞,有5款,占國產創新藥的一半以上。我國腫瘤市場巨大,根據弗若斯特沙利文的數據,2019年我國新增癌癥患者達440萬人,到2024年預計將達到500萬人。針對腫瘤領域大量未滿足的醫療需求,大批制藥企業將目光聚焦于腫瘤藥物的研發,不足為奇。
從靶點來看,有P-CAB、AR抑制劑、IKKα、PD-1單抗、PD-1/CTLA-4雙抗、MR拮抗劑、sGC刺激劑、JAK1抑制劑等熱門靶點。
腫瘤仍是第一大治療領域
今年上半年,多款抗腫瘤新藥在國內獲批上市,包括中藥1類新藥淫羊藿素軟膠囊,AR抑制劑瑞維魯胺片,以及兩款免疫檢查點抑制劑:斯魯利單抗和卡度尼利單抗。
我國癌癥負擔沉重,每年新發癌癥人數、死亡人數均居全球第一,腫瘤治療市場巨大。這些新藥的上市為我國腫瘤患者提供了新的治療選擇。
從具體產品類型來看,腫瘤免疫治療逐漸走上了舞臺,甚至走到了舞臺中央。
其中PD-1抑制劑是應用最為廣泛的免疫檢查點抑制劑。今年上半年就有兩款PD-1靶點新藥獲批,包括復宏漢霖的PD-1單抗斯魯利單抗和康方生物的PD-1/CTLA-4雙抗卡度尼利單抗。
截止目前國內上市的PD-1/PD-L1抗體已有14款,包括13款單抗和1款雙抗。

表2 國產PD-1單抗/雙抗
斯魯利單抗(H藥,商品名:漢斯狀)是復宏漢霖首款自主研發的PD-1抑制劑,用于經既往標準治療失敗的、不可切除或轉移性微衛星高度不穩定(MSI-H)的成人晚期實體瘤適應癥。斯魯利單抗聯合化療治療局部晚期或轉移性鱗狀非小細胞肺癌(sqNSCLC)和一線治療廣泛期小細胞肺癌(ES-SCLC)的NDA已獲得NMPA受理,此外,其治療小細胞肺癌(SCLC)也已獲得美國FDA孤兒藥資格認定。有望成為全球首個一線治療SCLC的抗PD-1單抗。
卡度尼利單抗(商品名:開坦尼)是康方生物自主研發的腫瘤免疫治療新藥PD-1/CTLA-4雙特異性抗體,適用于既往接受含鉑化療治療失敗的復發或轉移性宮頸癌患者的治療。這是全球首個獲批上市的腫瘤雙免疫檢查點抑制劑雙抗。
根據中國臨床腫瘤學會(CSCO)免疫治療專委會推出的《中國實體瘤免疫治療臨床應用現狀白皮書》,在參與調研的三甲醫院醫生中,有99%的醫生處方過免疫檢查點抑制劑,96%醫生認為免疫檢查點抑制劑是安全可控的。隨著更多國產免疫檢查點抑制劑的獲批,以及醫保的支持,未來免疫治療將得到更廣泛的應用。
但免疫治療也并不完美。免疫治療好的療效是基于優勢人群的,而可惜的是只有30%左右是優勢人群,所以開發免疫治療聯合療法及其它新的腫瘤治療手段仍然任重而道遠。
自免市場新藥迎來春天
自身免疫性疾病是僅次于癌癥的第二大治療領域,是生物醫藥領域最富的一個富礦。在這座富礦里,誕生了多款重磅炸彈藥,例如蟬聯多年“藥王”的阿達木單抗。
我國市場相對國際市場,長期以來由于支付能力不足、醫療診療能力的欠缺等原因,導致市場滲透率低。但近年來隨著藥品價格下降,以及醫保支持,自免市場增長非常迅速。
在診療端,自免科室建設、醫生隊伍培養持續加速,疾病診斷率逐年攀升;在支付端,在國家醫保局政策支持下,2020-2022年已有14個進口自免產品醫保生效;在產品端,跨國藥企新一代自免產品國內外上市時間間隔進一步壓縮。
今年上半年NMPA就批準了輝瑞公司按1類新藥申報的口服JAK1抑制劑阿布昔替尼片(abrocitinib,商品名:希必可/CIBINQO)上市,用于對其他系統治療(如激素或生物制劑)應答不佳或不適宜上述治療的難治性、中重度特應性皮炎成人患者。
阿布昔替尼片是高選擇性JAK1抑制劑,2021年9月,阿布昔替尼在英國首次獲批上市,用于治療成人和12歲以上青少年中重度特應性皮炎患者。2022年1月14日,阿布昔替尼在美國獲批上市,推薦劑量為100mg和200mg,曾獲FDA突破性療法和優先審評資格。
在中國,CDE早在2021年2月就受理了阿布昔替尼片的上市申請,同年3月將其納入優先審評,并實現了全球同步研發和同步注冊。2022年4月11日,阿布昔替尼片在中國獲批上市。
除了阿布昔替尼,今年另一款JAK抑制劑,來自艾伯維的烏帕替尼也收獲頗豐,接連斬獲3項適應癥:中重度特應性皮炎(AD)、中度至重度活動性類風濕關節炎和活動性銀屑病關節炎。
截至目前,我國已獲批的JAK抑制劑達5款,分別為:諾華的蘆可替尼、禮來的巴瑞替尼、輝瑞的托法替布、艾伯維烏帕替尼、輝瑞阿布昔替尼,適應癥主要覆蓋類風濕關節炎、骨髓纖維化、特應性皮炎等。
面對巨大的潛力市場,國內藥企也已經開始投入其中,但整個自免賽道與跨國藥企相比,還處于剛起步的階段。就JAK抑制劑而言,目前尚無國產JAK抑制劑獲批上市,但布局JAK抑制劑的創新藥企已有10余家,臨床進展較快的項目主要有:
恒瑞醫藥的JAK1抑制劑SHR0302,針對類風濕關節炎、強直性脊柱炎、銀屑病關節炎、特應性皮炎、斑禿、結腸炎等適應癥均已處于Ⅲ期臨床階段,且特應性皮炎適應癥已被納入突破性治療,有望成為首款國產JAK抑制劑。
澤璟制藥的JAK1/2/3抑制劑杰克替尼,針對骨髓纖維化、重癥斑禿適應癥均已處于Ⅲ期臨床階段;還有處于Ⅰ期臨床階段的輕中度斑禿、輕中度特應性皮炎等適應癥。
科倫博泰的JAK1/2抑制劑KL130008膠囊,針對類風濕性關節炎、重度斑禿適應癥已處于Ⅱ期臨床階段。
微芯生物的JAK3激酶抑制劑CS12192膠囊,迪哲醫藥的—JAK1選擇性抑制劑AZD4205膠囊,高光制藥的TYK2/JAK1雙抑制劑TLL-018片也已進入臨床階段。
相對抗腫瘤領域激烈的競爭,我國自身免疫性疾病市場尚屬藍海。但未來5-10年或將迎來行業黃金發展期,誰能破局成為引領行業的龍頭企業,我們將持續關注。
來源:藥智網
本文為本網轉載,出于傳遞更多信息之目的,并不意味著贊同其觀點或證實其內容的真實性,如涉及侵權,請權利人與本站聯系,本站經核實后予以修改或刪除。


請完善以下信息,我們的顧問會在1個工作日內與您聯系,為您安排產品定制服務
評論